DBV : un concurrent sérieux sort du bois
Aimmune Therapeutics obtient à son tour une Breakthrough Therapy Designation
La société Aimmune Therapeutics vient d'obtenir le statut de Breakthrough Therapy Designation (BTD) aux US pour son traitement AR101 dans l’allergie aux arachides - il s'agit de la 2e annonce de grande ampleur en deux semaines pour cette société non cotée. Son concurrent DBV Technologies avait obtenu le même statut BTD au mois d'avril. Les sociétés semblent désormais au coude-à-coude pour mettre sur le marché le premier traitement de l'allergie à l'arachide.
Aimmune avait publié des résultats positifs de Phase 2b sur son AR101 le 7 juin dernier, lors du Congrès de l'European Academy of Allergy & Clinical Immunology (EAACI). Au même moment, DBV avait également publié des résultats dans l'allergie alimentaire au congrès de l'EAACI , sur une analyse post-hoc dans la sous-population pédiatrique. À l'heure actuelle, si les deux sociétés ont un timing similaire, DBV a tout de même démontré un meilleur bénéfice / risque.
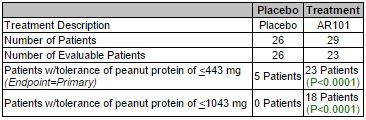
Résultats de Phase 2b d'Aimmune, sur l'AR101 (juin 2015):
Sur les 23 patients ayant pris l'AR101, 78% ont toléré l’ingestion d’une dose d’arachide 10x fois supérieure à ce qu’ils pouvaient endurer auparavant (1043 mg contre 100 mg au départ). Ces résultats sont meilleurs que ceux de DBV qui avait réussi à démontrer une efficacité chez 50% des patients (pour l'ingestion d’une dose d’arachide d’au moins 1000 mg).
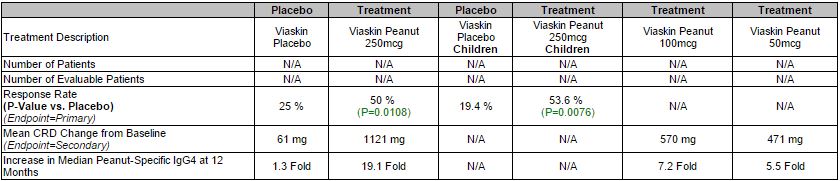
Résultats de Phase 2b de DBV, sur Viaskin Peanut (février 2015):
Les deux sociétés sont au coude-à-coude dans le développement du premier traitement de l'allergie à l'arachide : elles devraient lancer leur étude de Phase 3 au même moment aux US, fin 2015.
Pour le moment, avantage à DBV Technologies:
-l'essai de Phase 2 comportait davantage de patients par rapport à Aimmune (221 vs. 55);
-on a observé dans l'essai de Phase 2 d'Aimmune des effets secondaires (GI comme indiqué) mais aussi 1 Serious Adverse Event (choc anaphylactique ayant nécessité une injection d'épinéphrine) contre 0 SAE chez DBV Technologies
-et le patch de DBV est plus approprié (traitement oral chez Aimmune).
A l'avenir, il sera intéressant de savoir si les adolescents inscrits dans l'essai d'Aimmune ont eu des taux de réponse similaires à ceux des enfants. En outre, il sera également intéressant de savoir si des doses plus importantes d' AR101 (au-delà de la dose maximale testée) peuvent augmenter la tolérance du patient pour les arachides - certains experts estiment que les effets secondaires, notamment gastro-intestinaux (il faut savoir que 6 patients ont abandonné l'essai en raison de complications gastriques), peuvent mettre un frein à de nouvelles augmentations de doses. On attend le design de Phase 3 pour les 2 sociétés.
On suivra les prochains développements avec grand intérêt !
Newsflow attendu sur DBV au cours des prochains mois:
| Timing | Catalyseurs |
| 3e Trimestre 2015 | Annonce du futur design de la phase 3 pour Viaskin Peanut (allergie aux arachides). Le marché attend un design proche de celui de la phase 2, la probabilité de succès deviendra alors très importante |
| Octobre 2015 | Publication des résultats à 2 ans de l'étude VIPES |
| 4e Trimestre 2015 | Publication des résultats de Phase 2 de l’étude CoFAR chez 75 patients (essai multicentrique, randomisée, en double-aveugle contre placebo utilisant le Viaskin Peanut pour traiter les enfants et les adultes allergiques à l'arachide) |